Vitamina D și insuficiența renală cronică: interes reînnoit pentru o vitamină uitată
rezumat
Pacienții cu insuficiență renală cronică au o mortalitate care depășește cu mult rata prevăzută de factorii de risc cardiovascular convenționali. Deficitul de vitamina D, foarte răspândit în această populație, este, de asemenea, asociat independent cu mortalitatea. O mai bună înțelegere a fiziologiei vitaminei D a făcut posibilă evidențierea așa-numitelor funcții „extrarenale” ale acestei vitamine. Prin efectele sale cardiovasculare, de exemplu, substituția vitaminei D ar putea participa funcțional la reducerea mortalității în insuficiența renală. Acest articol rezumă cunoștințele despre vitamina D în insuficiența renală cronică și oferă recomandări privind screening-ul și substituirea vitaminei D la această populație cu risc.
Introducere
Rolul esențial al rinichiului în producerea formei active de vitamina D, 1,25-hidroxi-vitamina D3 (1,25 (OH) D3), este un concept vechi. Pierderea activității 1-α-hidroxilazei renale în CRF avansat este un element central în fiziopatologia hiperparatiroidismului secundar și a tulburărilor metabolice osoase legate de insuficiența renală (apoi prescurtată „boala osoasă renală”). Cu toate acestea, în ultimii cincisprezece ani, multe progrese științifice au schimbat profund înțelegerea fiziologiei vitaminei D. În special, a apărut că receptorul vitaminei D (VDR) a fost exprimat mult mai larg decât efectele osoase ale vitaminei „tradiționale”. a prezis. În plus, coexpresia VDR cu 1-α-hidroxilaza, enzima activatoare a vitaminei D, în multe țesuturi periferice, a dat naștere unui nou concept: forma activă a vitaminei D, 1,25 (OH) D3, poate să fie sintetizate în site-uri extrarenale și să genereze efecte autocrine locale. 7 Vitamina D joacă astfel un rol fiziologic în multe țesuturi, cum ar fi miocardul, mușchii, pancreasul, endoteliul, creierul și chiar celulele imune. 8.9
Vitamina D a devenit astfel un subiect esențial deja discutat în două recenzii excelente publicate în acest jurnal. 10,11 Acest articol de revizuire încearcă să descrie mai specific starea cunoștințelor cu privire la rolurile vitaminei D în CRF, atât în ceea ce privește metabolismul fosfocalcic, cât și efectele sale extra-osoase. Prima parte descrie biosinteza vitaminei D și analizează pe scurt rolul acesteia în fiziopatologia metabolismului fosfocalcic în CRF. A doua parte examinează funcțiile extra-osoase ale vitaminei D implicate în bolile renale. În cele din urmă, o secțiune practică finală oferă recomandări privind screening-ul și înlocuirea deficienței native de vitamina D la pacienții cu boli de rinichi.
Termenii „vitamina D nativă”, vitamina D sau colecalciferol vor fi folosiți sinonim și se vor referi la colecalciferol. Termenul "vitamina D activă" se va referi la calcitriol (1,25 (OH) D3). Calcidiolul sau calcifediolul este forma intermediară a vitaminei D după 25-hidroxilare hepatică (25 (OH) D3).
Rolul vitaminei D în fiziopatologia insuficienței renale
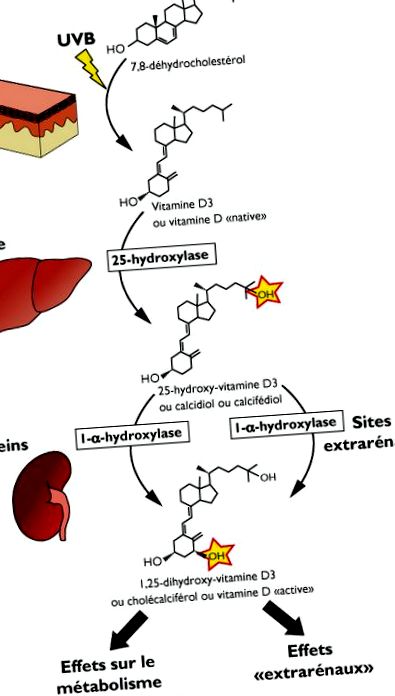
Biosinteza vitaminei D
Vitamina D și metabolismul fosfocalcic în insuficiența renală cronică
Vitamina D3 este cunoscută de mult timp pentru efectele sale osoase și rolul său în bolile osoase ale rinichilor este bine stabilit. Vitamina D activă acționează direct asupra creșterii absorbției intestinale și a reabsorbției tubulare renale a calciului, crește resorbția osoasă și inhibă secreția de PTH. Deficitul prelungit de vitamina D este cauza rahitismului la copii și a osteomalaciei la adulți. În CRF, pierderea masei nefronice este asociată cu o scădere a activității renale a 1-α-hidroxilazei și, prin urmare, la nivelul circulant de 1,25 (OH) D3. Acest lucru are ca rezultat un echilibru negativ al calciului și o creștere secundară a PTH (hiperparatiroidism secundar), responsabil de boala osoasă a rinichilor. Acest efect apare tardiv și este descris clasic în timpul etapei 3 a CRF (rata de filtrare glomerulară 14 În același timp, expresia FGF23 crește de la etapa 2 a CRF, promovând eliminarea fosfatului renal. Acest mecanism de adaptare timpurie păstrează homeostazia fosfocalcică prin prevenirea fosfatului plasmatic creșterea în stadiile incipiente ale CRF În stadiile avansate ale CRF, concentrația foarte mare de FGF23 ar putea fi dăunătoare, acționând ca o toxină uremică.
Mai mult, FGF23 inhibă secreția de 1-α-hidroxilază și PTH. 14 În schimb, creșterea de 1,25 (OH) D3 poate induce expresia Klotho. 14 Și în cerc complet, 1,25 (OH) D3 are un efect inhibitor bine descris asupra secreției de PTH. În cele din urmă, PTH stimulează producția de 1,25 (OH) D3 și FGF23. Uremia poate inhiba, de asemenea, hidroxilarea hepatică a vitaminei D prin scăderea producției de 25 (OH) D3. 16 Activitatea Klotho, FGF23, PTH și 1-α-hidroxilază interacționează astfel într-un mod complex pentru a menține calciu seric normal și a limita creșterea fosfatului plasmatic (Figura 2). Astfel, acestea influențează devreme metabolismul vitaminei D în CRF. Pe măsură ce insuficiența renală progresează, aceste mecanisme sunt totuși copleșite și fosfatemia crește (Figura 3). Hiperparatiroidismul persistent este responsabil pentru consecințele negative ale CRF asupra mineralizării osoase. Hiperfosfatemia și deficitul de vitamina D sunt doi candidați care pot explica excesul de mortalitate la pacienții cu CRF. 1.4
Boli renale cronice și deficit de vitamina D.
CRF în stadii incipiente este, de asemenea, un factor de risc semnificativ pentru deficitul de 25 (OH) D3. Prevalența insuficienței și deficienței vitaminei D este astfel de ordinul a 75% și respectiv 30% în insuficiența renală cronică 7, dar poate fi mult mai mare în anumite serii. 17 Prevalența deficitului de vitamina D crește odată cu înrăutățirea funcției renale, independent de vârstă, sex, greutate și rasă. 18 Scăderea în 25 (OH) D3 se corelează și cu scăderea în 1,25 (OH) D3, indiferent de stadiul insuficienței renale. 19 Scăderea în 25 (OH) D3 poate participa la scăderea în 1,25 (OH) D3 observată în stadiile avansate ale insuficienței renale, nu datorită activității scăzute a 1- α-hidroxilazei, ci pur și simplu printr-o scădere a substrat al acestei enzime. 12.19
Cauzele menționate sunt o expunere mai scurtă la soare într-o populație bolnavă, o dietă sărăcită în vitamina D sau o producție mai puțin eficientă de vitamina D3 de către piele, la fel ca persoanele de peste 70 de ani. Recent, un studiu sugerează, de asemenea, o scădere a activității 25-hidroxilazei hepatice legate de uremie. 16 Sindromul nefrotic este, de asemenea, o situație de risc ridicat pentru deficitul de vitamina D3, independent de pierderea funcției renale. Proteinuria ridicată la acești pacienți este însoțită într-adevăr de o scurgere urinară de 25 (OH) D3 legată de proteina de legare a vitaminei D (DBP). Apoi se poate dezvolta un deficit sever de vitamina D. 21 Acest mecanism apare probabil la orice pacient cu proteinurie semnificativă, de exemplu secundar nefropatiei diabetice.
Consecințele deficitului de 25 (OH) D3 sunt încă parțial înțelese doar în bolile renale. 25 (OH) deficit de D3 poate participa la complicațiile osoase ale CRF. Dar, fără îndoială, efectele sale extra-osoase sunt susceptibile de a explica o parte din excesul de mortalitate al pacienților cu CRF. 2-4
Efecte extraoase ale vitaminei D în bolile cronice de rinichi
Activarea locală a vitaminei D într-o mare varietate de țesuturi periferice este responsabilă de numeroasele sale efecte extrarenale raportate pe scară largă în literatură. 8,10 Fără a ne dori să fim exhaustivi, analizăm aici cele mai semnificative efecte non-osoase în IRC.
Efecte cardiovasculare
VDR se exprimă prin celule endoteliale, celule musculare netede și cardiomiocite. 22 Vitamina D pare, așadar, să joace un rol în reglarea presiunii arteriale, iar literatura de specialitate cu privire la acest subiect a fost recent revizuită în acest jurnal. 23 Cu toate acestea, deși unele studii clinice randomizate au demonstrat un efect benefic încurajator al substituției vitaminei D asupra controlului tensiunii arteriale, alte studii raportează rezultate contradictorii, care nu permit o concluzie definitivă. 23 De asemenea, este sugerat un efect benefic al vitaminei D asupra funcției cardiace și un studiu clinic a arătat o scădere a hipertrofiei ventriculare stângi la pacienții cu dializă după șase luni de tratament cu colecalciferol. 24 În plus, un studiu clinic multicentric randomizat și controlat (studiu PRIMO) este în curs de desfășurare pentru a evalua efectele paricalcitolului (un agonist VDR) asupra hipertrofiei ventriculare stângi la pacienții cu BCR, nu la dializă. 25 Funcția endotelială pare, de asemenea, să fie afectată direct de deficiența de vitamina D în CRF. 22.26
Efect antiproteinuric
Printre efectele non-osoase ale vitaminei D, efectul antiproteinuric al agoniștilor vitaminei D (calcitriol, paricalcitol) a atras recent atenția. Un posibil efect nefroprotector al vitaminei D3 a stârnit un oarecare entuziasm. Un studiu controlat randomizat (VITAL) a sugerat un efect antiproteinuric suplimentar al paricalcitolului în combinație cu un blocant al sistemului RAA (renină-angiotensină-aldosteron). Cu toate acestea, trebuie remarcat faptul că nu a fost evaluat niciun beneficiu la nivel de pacient, cum ar fi prevenirea progresiei CRF sau reducerea mortalității. În plus, populația observată a prezentat un deficit semnificativ în vitamina D3 nativă. Prin urmare, rămâne de definit dacă efectul antiproteinuric observat este specific paricalcitolului sau dacă o corecție a deficitului inițial de 25 (OH) D3 ar produce același efect.
Efect asupra sistemului imunitar
VDR și 1-α-hidroxilaza sunt exprimate de majoritatea celulelor sistemului imunitar. Activarea locală a vitaminei D poate astfel regla funcția imunitară, de exemplu prin îmbunătățirea răspunsului imun înnăscut antimicrobian. 9.28 Vitamina D poate avea, de asemenea, un efect antiinflamator sau imunomodulator. 28 de pacienți cu ERC prezintă un risc crescut de infecții și au frecvent microinflamare cronică. Cu toate acestea, asocierea acestor complicații cu deficiența de vitamina D și beneficiul unei substituții nu este stabilită.
Efect metabolic
VDR este prezent în celulele β ale pancreasului și vitamina D ar putea participa astfel la secreția de insulină, dar poate acționa și asupra sensibilității la insulină. 9 Similar cu pacienții fără CRF, nivelurile de 29,30 25 (OH) D3 se corelează invers cu rezistența crescută la insulină observată în CRF. 18 Un studiu clinic sugerează, de asemenea, un efect benefic al prescripției vitaminei D active asupra rezistenței la insulină la pacienții cu CRF non-diabetici. 31 Cu toate acestea, beneficiul substituției native a vitaminei D asupra rezistenței la insulină în CRF rămâne necunoscut.
Alte efecte
Celulele musculare scheletice au VDR și este necesară suficientă vitamina D pentru funcționarea lor optimă. Înlocuirea vitaminei D3 reduce astfel direct incidența căderilor. 32 de pacienți cu CKD sunt o populație în special cu risc de cădere și ar putea beneficia, de asemenea, de substituirea vitaminelor în acest sens. Cu toate acestea, un studiu clinic este încă necesar pentru a confirma un astfel de beneficiu. Vitamina D poate avea, de asemenea, un efect antitumoral frecvent descris, dar controversat. 9,10 CRF este, de asemenea, asociat cu un risc crescut de cancer, 33, dar nu există date care să stabilească o legătură între deficiența de vitamina D și incidența crescută a cancerului la această populație.
Vitamina D la pacienții cu insuficiență renală cronică, nu în dializă în practica clinică
Definiții
Nu există un consens stabilit cu privire la nivelul optim de 25 (OH) D3. Pentru majoritatea experților, o valoare de 25 (OH) D3 8,10
- Vitamina B12, ultimul ghid pentru vegetarieni; Vegetarian
- Vitamina B9 Surse și beneficii pentru organism Alvityl Algeria
- TOP 5 rețete pentru a umple cu vitamina D SOSCuisine
- Vitamina D pentru bebelușul tău Micii noștri mâncători
- Suplimente de vitamina D pentru creșterea performanței sportive