Pneumologul în managementul sclerozei laterale amiotrofice: spre mai puțin pesimism
rezumat
Pacienții cu scleroză laterală amiotrofică (SLA) necesită îngrijiri specializate și multidisciplinare. Insuficiența respiratorie rezultată din disfuncția musculară respiratorie, tusea ineficientă cu riscul de congestie, pierderea în greutate asociată cu disfagia și pierderea progresivă a autonomiei ar trebui să fie căutate și explorate sistematic. Sunt necesare doar câteva examinări suplimentare pentru a caracteriza un pacient cu SLA: funcții pulmonare, măsurarea gazelor, oximetrie nocturnă, debit de vârf al tusei, monitorizarea greutății. După ce a primit informații clare despre boala lor și despre avantajele și dezavantajele fiecărui tratament disponibil, pacientul va participa la deciziile de tratament. Acest articol trece în revistă diferitele etape ale managementului respirator pentru un pacient cu SLA.
Introducere
Scleroza laterală amiotrofică (SLA) afectează 2-3 persoane/100.000 de locuitori în fiecare an; prevalența sa este de 5-7/100.000 de locuitori. În marea majoritate a cazurilor, decesul rezultă dintr-un eveniment respirator. De fapt, SLA este asociată cu un risc ridicat de infecții bronhopulmonare secundare iterative favorizate de insuficiență respiratorie restrictivă și disfuncție glotică frecvent asociată. În ciuda unui prognostic care rămâne sumbru, există multe instrumente care pot contribui la un control mai bun al simptomelor, fie că este vorba de suport respirator, nutrițional sau de comunicare.
În acest articol vom discuta patru întrebări clinice importante:
LA. Există o disfuncție inspiratorie care necesită ventilație mecanică ?
B. Tusea este eficientă ?
VS. Implicarea bulbară permite o protecție adecvată a căilor respiratorii și continuarea nutriției orale ?
D. Sunt mijloacele puse în aplicare pentru a compensa dizabilitățile pacientului și a-și menține autonomia ?
Memento clinic
Boala apare sporadic în majoritatea cazurilor (95%). 3 Vârsta medie la debutul simptomelor este de 57 de ani. Prezentarea clinică obișnuită este cea a unui deficit motor pur care combină risipa musculară și fasciculările. Este cauzată de deteriorarea primului și celui de-al doilea neuron motor, care determină prezentarea clinică a bolii. În faza inițială, forma coloanei vertebrale se distinge de obicei de forma bulbară, înainte ca boala să progreseze la o formă completă. În 5% din cazuri, prezentarea inițială este cea a insuficienței respiratorii sau a hipoventilației alveolare nocturne. 4,5 După un examen clinic detaliat, diagnosticul se face printr-o electroneuromiogramă. Tratamentul cu riluzol este indicat în primele forme de SLA pentru a prelungi viața cu un beneficiu estimat de două până la șase luni. 6 Alte tratamente oferite uneori (creatină, α-tocoferol) nu s-au dovedit a fi eficiente. De preferință, pacientul trebuie trimis la o consultație multidisciplinară pentru a asigura îngrijiri coordonate, progresive și adecvate pentru stadiul său de afectare. 7
Există o disfuncție inspiratorie care necesită ventilație mecanică ?
Disfuncția inspiratorie în SLA rezultă în primul rând din implicarea diafragmatică. Implicarea mușchilor inspiratori limitează expansiunea cutiei toracice și explică sindromul restrictiv. Insuficiența respiratorie se manifestă inițial în timpul somnului și mai ales în somnul REM (mișcare rapidă a ochilor): ventilația se bazează apoi doar pe o diafragmă disfuncțională, în timp ce activitatea altor mușchi inspiratori este inhibată. 8 Când disfuncția diafragmatică atinge un nivel critic, provoacă hipoventilație alveolară definită de prezența hipercapniei.
Explorarea unei posibile disfuncții diafragmatice
Examinarea nu trebuie doar să caute dispnee la efort sau în repaus, ci și prezența ortopneei suficientă pentru a ridica indicația de ventilație neinvazivă (NIV) în SLA. 9,10 În mod sistematic, istoricul ar trebui să exploreze prezența tulburărilor de somn (treziri nocturne sufocante, somn fără odihnă, hipersomnolență în timpul zilei, dureri de cap dimineața) care pot fi primele semne ale insuficienței respiratorii. 11 În cele din urmă, ar trebui căutate simptome mai subtile care sugerează tulburări respiratorii în timpul somnului - dificultăți de concentrare, scăderea funcțiilor intelectuale, tulburări de memorie, iritabilitate neobișnuită, sindrom depresiv sau de anxietate -.
Diferitele examinări funcționale efectuate în mod curent pentru explorarea disfuncției diafragmatice sunt rezumate în Tabelul 1.
Examinări de rutină sugerate pentru diagnosticul disfuncției diafragmatice
Măsurarea inspirațională a presiunii
PI-max (presiunea inspiratorie maximă măsurată la gură la capacitatea funcțională reziduală) și SNIP (presiunea inspiratorie nazală) sunt măsuri simple ale forței globale a mușchilor inspiratori. Cu toate acestea, PI-max este adesea inadecvat pentru pacienții cu SLA predominant bulbar. Prin urmare, SNIP este adesea preferat, o manevră naturală care este mai ușor de efectuat cu o sondă de presiune nară. 12.15
Gasometrie
Analiza gazelor din sânge este esențială în managementul respirator al unui pacient cu MNM (boală neuromusculară), deoarece permite detectarea precoce a hipoventilației alveolare diurne. Odată cu progresul disfuncției mușchilor respiratori, hipercapnia, prezentă inițial în timpul somnului, se regăsește și în timpul zilei.
Studiul somnului
La pacienții cu SLA, primele probleme respiratorii apar în timpul somnului. O oximetrie nocturnă efectuată acasă permite deja suspectarea perioadelor de hipoventilație atunci când se observă perioade prelungite (> 5 min) de desaturare (SpO2 16 În prezent, realizarea unei polisomnografii nu este necesară pentru a începe o ventilație care nu este invazivă, dar sunt în curs studii determinați dacă detectarea precoce a evenimentelor respiratorii nocturne ar modifica managementul ventilator al acestor pacienți.Detectarea hipoventilației alveolare nocturne se bazează pe analiza transcutanată a PCO2 (capnografie), care trebuie efectuată în mod obișnuit în studiile de somn la pacienții cu SLA.
Tratamentul disfuncției diafragmatice
Ventilație mecanică neinvazivă
Scopul tratamentului mecanic este de a compensa eșecul mușchilor respiratori. În mod ideal, ar trebui să fie inițiat electiv, ca parte a unei monitorizări trimestriale a bolilor respiratorii, atunci când sunt îndeplinite criteriile de inițiere a ventilației neinvazive (NIV) (Tabelul 2). 17 Prea des, inițierea NIV are loc în timpul unui eveniment acut, în timpul spitalizării sau în terapie intensivă. În ciuda existenței recomandărilor experților, prea puțini pacienți beneficiază de evaluarea și managementul respiratorului specializat și precoce. 18 În Elveția, Pautex și colab. au arătat în recentele lucrări retrospective că doar o treime dintre pacienții cu SLA, urmată la Spitalul Cantonal din Geneva între 1996 și 2002, au beneficiat de NIV, în timp ce 83% dintre aceștia erau simptomatici din punct de vedere respirator. 19
Criterii pentru inițierea ventilației neinvazive în contextul unei patologii restrictive în conformitate cu chestiunea conferinței consens 1999
Tusea permite eliminarea secrețiilor traheobronșice ?
Interesul pentru mușchii expiratori (rect, oblic, intercostali interni) este mai recent. Atacul lor în contextul SLA contribuie la scăderea eficacității tusei și a fonației. În realitate, sunt necesare trei etape succesive pentru producerea unei tuse eficiente: inspirația inițială a unui volum mare de aer, dezvoltarea unei hipertensiuni intratoracice pozitive împotriva unei glote închise și deschiderea bruscă a glotei.asigurarea expulzării secrețiilor. . O tuse eficientă necesită, prin urmare, atât mușchi inspiratori și expiraționari eficienți, cât și o coordonare fină între funcțiile glotice și respiratorii.
Explorarea unei posibile disfuncții a mușchilor expiratori
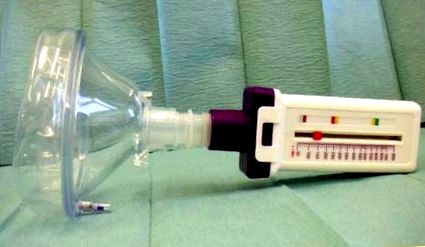
Este suficient să îi cereți pacientului să tusească pentru a realiza foarte repede eficacitatea tusei sale și riscurile de congestie bronșică. Debitul de tuse de vârf este un test simplu, reproductibil, care este utilizat zilnic în practica noastră clinică (Figura 2). Un debit de vârf de tuse mai mic de 170 l/min nu permite o tuse eficientă, 23 în timp ce un debit de vârf de tuse de peste 270 l/min este asociat cu un risc de congestie minimă.
Tratamentul pentru disfuncția tusei
În practică, se recomandă ședințe de fizioterapie respiratorie care combină diverse tehnici pentru a facilita drenajul periferic al secrețiilor și decongestionarea bronșică. S-au dezvoltat tehnici de stocare a aerului, folosind fie un Ambu, fie NIV pentru a crește volumul de aer inspirat, debitul expirator și astfel optimiza golirea traheală. Dacă acest lucru nu este suficient, se adaugă frecvent un ajutor mecanic pentru tuse (Figura 3) la arsenalul terapeutic. Asistența la tuse și-a demonstrat în mod clar eficacitatea la pacienții cu SLA. Mustfa și colab. rețineți, de exemplu, o creștere a debitului de vârf la tuse de aproape 30% la pacientul non-bulbar și de aproape 20% la pacientul bulbar cu un efect mai accentuat la pacienții cei mai grav afectați. 24 Învățarea asistenței la tuse este ușoară pentru kinetoterapeutul responsabil al pacientului, necesitând aproximativ o oră de antrenament; tehnica poate fi stăpânită și de rude fără pregătire paramedicală.
Implicarea bulbară permite continuarea nutriției orale și o protecție suficientă a căilor respiratorii?
Nu este necesară o examinare suplimentară pentru a decide asupra unei gastrostomii de hrănire. Cu toate acestea, această acțiune trebuie discutată cu pacientul atunci când CV-ul său depășește 50% din valoarea prezisă, pentru a reduce riscul de complicații respiratorii în timpul procedurii. În principiu, PEG va fi plasat percutan sub control endoscopic și sedare, supravegheat de un anestezist. În unele centre, gastrostomia radiologică percutană (PRG) pare a fi în prezent metoda preferată, deoarece rata sa de succes este mare și sedarea nu este în general necesară. 28,29
Sunt mijloacele puse în aplicare pentru a compensa dizabilitățile pacientului și a-și menține autonomia?
Logopedia trebuie oferită în mod sistematic pacienților de îndată ce apar tulburări de înghițire sau de fonație. Obiectivul nu este recuperarea funcțiilor pierdute, ci adaptarea la noile deficiențe. Reabilitarea va implica mobilizarea activă a mușchilor sferei orofaciale. Atunci când comunicarea orală nu mai este posibilă, vor fi oferite apoi alte mijloace mai adecvate: scriere, tabele de desemnare, tastatură de calculator, software de comunicare cu sinteză vocală. În Elveția, fundația teleteze (www.fst.ch) își propune să ofere persoanelor cu dizabilități tehnologii adaptate nevoilor lor. De asemenea, participă la dezvoltarea de produse performante și la adaptarea acestora la fiecare persoană cu dizabilități.
Terapeutul ocupațional ar trebui să fie implicat de îndată ce apare un disconfort funcțional cu repercusiuni asupra autonomiei (toaletă, pansament, mâncare, utilizarea unei tastaturi etc.). El va putea participa la testele de echipament. El va fi, de asemenea, responsabil pentru instruirea altor îngrijitori pentru a se adapta la mediul pacientului cu SLA. În cele din urmă, va putea juca un rol cheie în adaptarea locuinței la nivelul dizabilității. Doar cu prețul vizitelor regulate la domiciliu, cu o adaptare progresivă a acestuia din urmă la progresia handicapului, va fi posibilă menținerea pacientului în locul său de viață.
Indiferent de planul de tratament oferit pacienților cu SLA, aceștia vor putea lua o decizie în cunoștință de cauză numai atunci când li s-au furnizat informații detaliate despre boala lor. Aceste informații obiective despre evoluția bolii ar trebui să fie regula. Avantajele și dezavantajele suportului ventilator, ale PEG sau ale ajutoarelor mecanice pentru tuse trebuie discutate. Alegerile pacientului nu vor fi definitive și pacientul ar trebui să se simtă liber să se răzgândească. Acesta este modul în care principiul autonomiei pacientului este cel mai bine respectat, iar pacientul este, de asemenea, invitat să scrie directive în avans. El poate fi ajutat în acest proces de către medicul curant sau de o echipă specializată în îngrijiri paliative. 30 Împotriva unei abordări excesiv de paternaliste, mai mult de 95% dintre pacienți sunt în favoarea directivelor avansate. 31
Concluzie
SLA rămâne o boală neurodegenerativă cu prognostic dramatic. Diagnosticul poate fi făcut inițial de către un medic generalist, care este, de asemenea, responsabil pentru orchestrarea ulterioară a unui consult multidisciplinar care îmbunătățește gestionarea acestor cazuri grave. Multe intervenții medicale s-au dovedit a fi eficiente atât în prelungirea vieții pacienților, cât și în îmbunătățirea calității vieții acestora. Foarte des, aceste intervenții se referă la pneumolog care joacă un rol cheie într-un consult multidisciplinar pentru managementul SLA. Misiunea acestuia din urmă va fi evocarea, explorarea și tratarea diferitelor fațete ale insuficienței respiratorii.
implicatii practice
> Scleroza laterală amiotrofică (SLA) este o boală neurologică degenerativă cu prognostic slab. În timpul vizitelor medicale regulate, trebuie căutate sistematic mai multe puncte:
ortopnee, care este suficientă pentru a face indicația ventilației neinvazive în SLA. Indicația pentru ventilația neinvazivă este pusă și de asocierea unui simptom respirator și cel puțin unul dintre următoarele elemente: capacitate vitală Toate mijloacele de compensare pentru dizabilitățile pacientului vor fi implementate pentru a asigura întreținerea acasă cât mai mult posibil
> Principiul autonomiei pacientului trebuie respectat. Acesta din urmă este invitat să scrie directive în avans, în special pentru a clarifica atitudinea în timpul internărilor de urgență
Bibliografie
Abstract
Este necesară îngrijire specializată și multidisciplinară pentru pacienții cu scleroză laterală amiotrofică (SLA). Insuficiența respiratorie secundară disfuncției musculare respiratorii, tuse ineficientă, pierderea în greutate și pierderea progresivă a autonomiei ar trebui întotdeauna căutate și explorate. Sunt necesare foarte puține teste pentru a evalua un pacient cu SLA: spirometrie, gaze din sânge, oximetrie nocturnă, flux de vârf al tusei și urmărirea greutății corporale. Pacienții trebuie informați în mod clar cu privire la natura și evoluția SLA și cu privire la potențialele beneficii și dezavantaje asociate fiecărei modalități de tratament pentru a fi implicați în deciziile terapeutice. Această revizuire bazată pe dovezi se concentrează pe îngrijirea respiratorie a pacienților cu SLA.
- Obiceiuri de adoptat în gestionarea constipației ocazionale Microlax®
- Rolul reabilitării cardiace multidisciplinare în managementul pacientului afectat
- Boli tiroidiene UPGCS denunță un tratament nepotrivit pentru experiența pacienților
- Lipoedem, 12 litri de grăsime din coapse sunt îndepărtați
- Lipofilling de sân - Injecție de grăsime în sâni Dr. Natalie Rajao Paris