Știri despre biocampus
Starea de sănătate a modelului „rozătoarelor” în cercetare
La începutul secolului al XX-lea, un cercetător a spus „Nu pot să fac experimentul meu pentru că animalele sunt moarte”
La mijlocul secolului al XX-lea, un cercetător a spus „Nu pot să-mi fac experimentul, deoarece animalele sunt bolnave”
În secolul 21, cercetătorul declară „Nu pot să îmi fac protocolul, deoarece animalele sunt infectate”
Adaptat din DG Baker. Recenzii clinice de microbiologie, apr. 1998, p. 231–266
În funcție de teme și proiecte de cercetare, este necesar să se definească „modelul” cel mai potrivit. Genetica (genotipul: fundal genetic + mutație în cazul OMG-urilor) și mediul sunt elemente care fac parte integrantă din model deoarece determină fenotipul.
În parametrii de mediu găsim starea de sănătate, deci înțelegem că poate influența fenotipul. Situația este complicată atunci când vrem să cunoaștem gradul de influență al stării de sănătate asupra fenotipului observat. Din acest motiv, utilizarea unui standard de sănătate (deoarece există standarde genetice) este crucială deoarece „limitează”, pe cât posibil, variațiile cauzate de starea de sănătate în rezultatele comparate. Acestea fiind spuse, este foarte posibil să nu se utilizeze un astfel de standard, dar în acest caz, acesta devine un parametru complet al experimentului, în special deoarece poate genera o variabilitate foarte mare a rezultatelor obținute.
Astfel, reproductibilitatea și compararea rezultatelor în comunitatea științifică necesită definirea standardelor care ar trebui alese în funcție de scopul studiilor lor. Standardul european de referință este stabilit de FELASA (Federația Asociațiilor Europene de Știință a Animalelor de Laborator) care funcționează sub forma unor recomandări care definesc și recunosc doar statutul SPF (EOPS) și SOPF. Fiecare stare de sănătate corespunde unei liste de excludere, adică o listă a agenților infecțioși care trebuie să lipsească de la unitatea animală. Statutul „convențional” se bazează pe o listă de excludere care conține doar agenți zoonotici majori (zoonoză: boală care poate fi transmisă de la animale la oameni sau de la oameni la animale). Statutul SPF ia în considerare principalii agenți patogeni la rozătoare și, prin urmare, face posibilă stabilirea unei stări de sănătate pentru animalele „sănătoase”, libere de agenții patogeni principali. Statutul SOPF include în lista sa de excludere agenți ai statutului SPF la care se adaugă oportunistii.
Pentru a menține starea de sănătate în timp, este necesar să se stabilească bariere (cu atât mai importante cu cât statutul este ridicat) și să se asigure monitorizarea sănătății animalelor prezente pentru a verifica excluderea agenților doriți (în funcție de tip statutul dorit) și să garanteze starea de sănătate.
Este imposibil să se evalueze cu certitudine dacă o stare de sănătate este potrivită pentru experimentele sale. Acestea fiind spuse, principiul nu este să „excludem totul” sau „să acceptăm totul”, ci să avem „o listă de excludere” pe baza:
- Agenții pe care îi testez (identificăm și evaluăm doar ceea ce căutăm).
- Dintre acești agenți testați, care sunt tolerați în magazinul meu de animale de companie și care trebuie excluși în funcție de tipul de cercetare efectuată. Atenție: majoritatea agenților care interferează cu rezultatele experimentale nu sunt responsabili pentru semnele clinice la rozătoare. Cu alte cuvinte, mouse-ul poate părea perfect sănătos și un model animal foarte sărac. Acesta este motivul pentru care screeningul regulat este esențial.
Într-un institut de cercetare, vor exista în esență două constrângeri:
- Interinstitute: să poată efectua experimente în condiții care să permită reproductibilitatea cu alte institute care utilizează aceleași standarde (standarde).
- Intra-institut: Pentru a permite tuturor să aibă animale cu un statut compatibil cu experimentele lor, în ciuda multidisciplinarității Institutului.
Acest lucru poate trece printr-o unitate de animale cu o rată ridicată de excludere pentru a se potrivi tuturor, dar cu constrângeri logistice semnificative sau prin multiplicarea zonelor separate (cu bariere de sănătate) care acoperă mai multe stări de sănătate.
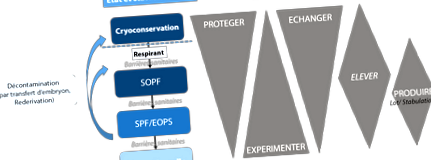
Figura 1: starea de sănătate cea mai potrivită în funcție de nevoie. În albastru: organizarea statului (crioconservarea și respirația animalelor) și starea de sănătate. Integritatea fiecărei zone este menținută datorită barierelor sanitare. Fluxul de animale este de la SOPF la convențional, pe de altă parte, revenirea la un statut superior este posibilă numai prin decontaminare. În gri: utilizarea modelului în funcție de starea de sănătate. Un model este mai ușor protejat și schimbat dacă este crioconservat și/sau în stare SOPF, pe de altă parte, experimentarea este mai ușoară (flux și barieră mai simplă) în starea de sănătate convențională sau SPF/EOPS. Reproducerea și producția pe loturi vor fi cu atât mai ușurate atunci când animalele se află într-o stare bună de sănătate și, prin urmare, se află într-o stare mai mare de SOPF și SPF. Acest principiu ar trebui adaptat în funcție de proiectele de cercetare și de sensibilitatea acestora la starea de sănătate.
În primul rând, luând în considerare bunul simț, reglementările și etica, a avea animale în stare bună de sănătate și a nu purta agenți patogeni este esențial și este pe deplin în conformitate cu regula 3R (menținerea unui sănătos și productiv). În plus, există considerații economice asociate cu pierderea unui model din motive de sănătate și incapacitatea de a exploata rezultatele experimentale. În cele din urmă, un standard de sănătate oferă posibilități mai bune pentru schimbul de animale între angajați.
Acum ce să răspundem la întrebarea: „care agent va influența experimentele mele?” "
În primul rând, este important de remarcat faptul că deficiențele genetice prezente în liniile de OMG-uri își pot modifica susceptibilitatea la agenți oportunisti și/sau simbiotici (microbiota) și astfel pot duce la apariția „patobioniților” în mod normal, fără impact asupra stării de sănătate.
În general, se înțelege că lista nu va fi exhaustivă și cu părtinire în funcție de scopul fiecăruia și de prevalența agenților infecțioși în instalațiile pentru animale. Acestea fiind spuse, veți găsi mai jos un tabel care încearcă să stabilească „câmpuri” de interferență la căutare în funcție de agenții găsiți (sursa https://www.inserm.fr/sites/default/files/media/ entity_documents/Inserm_RecommandationsEtablissementsExperimentationAnimale_2009. pdf).
Deși este destul de ușor de înțeles că multe microorganisme vor avea o influență asupra imunologiei sau asupra sistemului digestiv și respirator, pentru alte domenii putem cita, de exemplu:
- Parvovirus care previne creșterea tumorii în studiile oncologice.
- Encephalitazoon Cuniculi și diferiți viruși la șoareci (MVM, TMEV, LCMV și MAD1), care acționează asupra sistemului nervos central, vor avea un impact asupra studiilor de neurobiologie.
- Se știe că MHV are o interferență foarte puternică în diferite zone, începând cu zootehnica și creșterea animalelor.
Virusul Ectromelia, MHV, EDIM, mAdV, Reo3, Helicobacter sp., Citrobacter rodentium, Clostridium piliformis, Giardia muris, Spironucleus muris, Syphacia muris, Syphacia oblevata, Aspicularis tetraptera, Emeria sp., Encephaliitozoon cunia
Virusul Ectromelia, LCMV, MHV, MVMp & i, MPV, Reo3, Sendai virus, Helicobacter sp., Citrobacter rodentium, Corynebacterium kustcheri, Encephalitozoon cuniculi, Mycoplasma sp. (pulmonis)
Virus Ectromelia, MHV, MPV, MVMp & i, LCMV, Sendai virus, PVM, Reo3, Myobia musculi, Radfordia affinis, Myocoptes musculinus, Citrobacter rodentium, Corynebacterium kustcheri, Encephalitozoon cuniculi, Mycoplasma sp. (pulmonis), Syphacia muris, Syphacia oblevata, Aspicularis tetraptera, Giardia muris, Spironucleus muris, Staphylococcus aureus
- Abonament scrisoare de reziliere Fitnext - șablon PDF și Word
- Urmăritori d; activitate care model pentru care se utilizează
- Scrisoare de reziliere gratuită - șablon de scrisoare gratuită
- Ursul Grizzly ar putea ajuta cercetarea diabetului
- Secretele dietetice ale lui Jennifer Hudson - Blogul