Locul nucleotidelor în nutriția clinică
rezumat
Nucleotidele și derivații lor sunt implicați în majoritatea proceselor biochimice și, prin urmare, joacă un rol important în metabolismul celular. Deși acești compuși pot fi sintetizați sau reciclați de organism, în anumite condiții, este necesară o sursă exogenă pentru a acoperi nevoile organismului. S-au dezvoltat soluții nutritive enterale și parenterale îmbogățite cu nucleotide din rezultatele preclinice. Aceste soluții comercializate și-au demonstrat eficacitatea, în special, prin îmbunătățirea funcției intestinale și a capacității de a depăși mai rapid traumatismele chirurgicale. În ciuda acestor efecte benefice, utilizarea lor poate prezenta riscuri pentru anumite tipuri de pacienți. Astfel, ar putea fi important să reconsiderăm potențialul acestor nutrienți în reducerea complicațiilor post-chirurgicale.
Introducere
Acizii nucleici și constituenții lor principali, nucleotidele, sunt rareori luate în considerare în managementul nutrițional al pacientului. Acest lucru se datorează probabil faptului că nucleotidele nu sunt substanțe nutritive esențiale, deoarece pot fi sintetizate de novo în celule din carbohidrați și aminoacizi. Prin urmare, nu există recomandări specifice cu privire la aportul zilnic al acestora. Cu toate acestea, nucleotidele joacă un rol esențial în metabolismul celular, deoarece acestea sunt implicate în majoritatea proceselor biochimice. Studii recente arată că un aport alimentar de nucleotide poate avea, în anumite patologii, un impact asupra sistemului imunitar și al trofismului intestinal. Obiectivul acestei revizuiri este de a oferi o imagine de ansamblu asupra mecanismelor de acțiune și a potențialului acestor nutrienți în managementul nutrițional al pacientului.
Structura și nomenclatura nucleotidelor
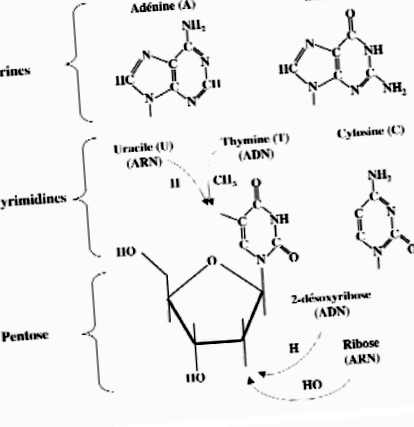
Nucleotidele sunt esteri fosfatici ai pentozei. Acestea sunt compuse din zaharuri cu cinci atomi de carbon (pentoză) din care carbonul 1 'este conectat la o bază organică și carbonul 5' la o grupare fosfat. Baza lor organică este o moleculă aromatică heterociclică plană. Este alcătuit fie din două inele condensate (purină), fie dintr-un singur inel (pirimidină). Prezența atomilor de azot în inele le conferă un caracter de bază, deși nicio bază nu este protonată la pH neutru. Caracterul acid al nucleotidelor se datorează de fapt prezenței grupării fosfat, care se disociază în condiții fiziologice. În absența acestora din urmă, moleculele compuse doar dintr-o bază și un zahăr sunt numite nucleozide. Celulele și mediul extracelular conțin o cantitate mică. Principala diferență între ARN (riboză) și ADN (dezoxiriboză) este tipul de pentoză nucleotidică. Cealaltă diferență este înlocuirea unei baze pirimidice în ARN (uracil) cu alta în ADN (timină) (fig. 1). Tabelul 1 prezintă nomenclatura celor patru tipuri de ribonucleozide și dezoxiribonucleozide.
Sinteza nucleotidelor
Majoritatea celulelor animale își sintetizează purinele și pirimidinele de novo din compuși simpli de carbon și azot, mai degrabă decât din purine și pirimidine preformate. Acești compuși sunt furnizați de precursori, cum ar fi CO2 sau tetrahidrofolat pentru compuși de carbon și glutamină sau aspartat pentru compuși de azot. Zahărul este obținut de la un precursor, 5-fosforibozil-1-pirofosfat (PRPP), provenind din calea sintetică a pentozei fosfați.
Sinteza de novo a purinelor are ca rezultat mai întâi formarea inozinei-5'-monofosfatului (IMP). Acesta din urmă poate fi transformat în AMP sau GMP prin două reacții distincte. AMP și GMP sunt apoi fosforilate de două ori în ATP și GMP. Aceste reacții se autoreglează retroactiv, deoarece sinteza AMP și GMP necesită adăugarea unei grupe amino în prezența, respectiv, a GTP și ATP (fig. 2).
De asemenea, nucleotidele pirimidinice sunt sintetizate de novo de la un precursor cheie, UMP. Pe de o parte, acesta din urmă poate fi transformat în UTP prin două fosforilări consecutive, apoi în CTP prin adăugarea unei grupări amino. Pe de altă parte, UMP după ce a fost transformat în dUMP de ribonucleotid reductază (RR), este metilat în dTMP de timidilat sintetază (TS) (fig. 3).
De fapt, dezoxiribonucleotidele pentru sinteza ADN sunt toate obținute prin reducerea nucleotidelor prin RR.
Deși celulele preferă să utilizeze sinteza nucleotidică de novo, acesta din urmă consumă multă energie sub formă de ATP și poate fi prea scump în anumite condiții. De exemplu, în timpul stresului metabolic sau al creșterii rapide a țesuturilor în care cererea depășește capacitatea intrinsecă de sinteză de novo, celulele utilizează direct purine și pirimidine de origine exogenă sau din catabolismul acidului nucleic. Calea de recuperare a purinei utilizează în special adenin fosforibosil transferaza (APRT) pentru a forma AMP din adenină și hipoxantină guanină fosforbosil transferază (HGPRT) pentru a forma GMP din guanină (fig. 2). Același lucru este valabil și pentru calea de recuperare a pirimidinei, unde, de exemplu, timidin kinaza (TK) fosforilează timidina de origine exogenă în dTMP (fig. 3).
Metabolismul nucleotidelor alimentare
Efectele nucleotidelor asupra sistemului imunitar
Influența nucleotidelor asupra sistemului imunitar este importantă. Funcționează prin promovarea proliferării, diferențierii și maturării celulelor imune, cum ar fi macrofagele, limfocitele T și neutrofilele. Mecanismele de acțiune ale nucleotidelor nu sunt însă complet elucidate, mai ales că cantitatea de nucleotide cu efecte imunomodulatoare este foarte mică în comparație cu cantitățile de ATP și ARN prezente în organism. 1
Mai multe studii in vitro și in vivo au încercat să înțeleagă aceste mecanisme de bază. În studiile in vitro, s-a raportat că un tip de celulă stimulat de nucleotide poate induce consecutiv activarea unui alt tip sau subtip de celule. Nucleotidele probabil au activat macrofagele prin stimularea proliferării celulelor T helper. 2
În plus, s-a propus că nucleotidele pot activa celulele imune prin inducerea secreției mediatorilor chimici și stimularea expresiei receptorului lor. Interleukina 2 (IL-2) a fost descrisă în special ca inducând proliferarea și expansiunea clonală a subtipurilor de celule T, stimulându-le să progreseze de la faza G1 la faza S a ciclului celular. Astfel, s-a sugerat că suplimentarea cu nucleotide stimulează proliferarea neutrofilelor prin creșterea secreției de IL-2 și a expresiei receptorului său. 2
Rezultatele obținute in vitro au fost confirmate in vivo. Într-un model de neutropenie murină indusă de ciclofosfamidă, aportul alimentar de nucleotide a contribuit la stimularea proliferării, diferențierii și maturării neutrofilelor periferice. 3,4 Suplimentarea cu nucleotide prin adăugarea de ARN sau uracil la o dietă fără nucleotide a făcut, de asemenea, posibilă recuperarea răspunsului limfoproliferativ la mitogeni, măsurat prin indurație și eritem dermic. 2,5 În schimb, o dietă fără nucleotide a redus expresia IL-2, a interferonului gamma și a markerului de suprafață celulară Lyt-1. 2
Unele rezultate sugerează că pirimidinele joacă un rol mai important în răspunsul imun decât purinele. 2 Într-adevăr, s-a raportat că suplimentarea cu uracil singură ar putea reproduce acțiunea unui amestec complet de nucleotide (ARN) prin creșterea supraviețuirii șoarecilor Balb/c după inoculare cu Staphylococcus aureus. În schimb, suplimentarea cu adenină singură nu a avut niciun efect. 3.6
În cele din urmă, nucleotidele par să acționeze la mai multe niveluri asupra sistemului imunitar. În răspunsul inflamator, acestea stimulează atât răspunsul celulelor T helper la antigeni, transformarea blastelor, proliferarea celulară și generarea de celule efectoare, precum și eliberarea factorilor chimiotactici și a limfokinelor, care la rândul lor amplifică răspunsul. sau au funcții efector directe (fig. 4).
Efectele nucleotidelor asupra sistemului digestiv
În condiții fiziologice normale, celulele gastro-intestinale sunt în mod natural mai expuse la nucleotide din alimente decât alte celule din corp. Prin urmare, nu este surprinzător faptul că utilizarea soluțiilor nutritive artificiale a demonstrat importanța unei surse exogene de nucleotide asupra trofismului mucoasei intestinale (fig. 4).
De exemplu, s-a raportat că nutriția enterală lipsită de nucleotide scade semnificativ greutatea mucoasei jejunale, adâncimea criptelor și înălțimea vilozității, comparativ cu nutriția orală normală. 7 În schimb, adăugarea de nucleotide în nutriția enterală a făcut posibilă creșterea adâncimii criptelor și a înălțimii vilozităților după inducerea diareei printr-o dietă pe bază de lactoză, 7 îmbunătățirea trofismului intestinal și reducerea translocației bacteriene induse de endotoxină în șoarecii cărora li s-a administrat o dietă fără proteine. 8
S-a demonstrat că nutriția parenterală are impact asupra trofismului mucoasei intestinale. Într-adevăr, un studiu a arătat că absența hranei intraluminale, datorită nutriției parenterale de lungă durată, a provocat atrofia mucoasei intestinale mult mai importantă decât în timpul hranei enterale. 9 Adăugarea de nucleotide în nutriția parenterală a făcut din nou posibilă refacerea greutății, a activității enzimatice de suprafață și a concentrației de proteine și acizi nucleici în mucoasa intestinală la șobolan. 10
Sensibilitatea celulelor gastro-intestinale la nucleotidele alimentare nu este surprinzătoare, deoarece aceste celule, mai mult decât oricare alta din corp, sunt literalmente scufundate într-un ocean de nucleotide active fiziologic, jucând un rol fundamental în funcțiile celulare și tisulare. În plus, s-a demonstrat că celulele gastro-intestinale prezintă deficiențe în calea biosintetică de novo a purinelor și pirimidinelor. Prin urmare, aceste celule epiteliale ar putea depinde de o sursă exogenă de nucleotide, 13 necesare sintetizării acizilor nucleici prin calea de recuperare a nucleotidelor pentru proliferarea și diferențierea acestora. 14 Aceasta explică de ce suplimentarea cu nucleotide la șobolani hrăniți cu nutriție parenterală a modulat răspunsul imun, a promovat vindecarea intestinală mai rapid și a îmbunătățit trofismul intestinal, la concentrații mult mai mici decât glutamina, principalul substrat pentru sinteza de novo a nucleotidelor. 1
Alte efecte ale nucleotidelor
Efectele suplimentării cu nucleotide nu se limitează doar la răspunsul imun și la mucoasa intestinală. Un aport exogen de nucleotide a facilitat, de exemplu, recuperarea contractibilității miocardice în modele de reperfuzie cardiacă. La câinii care au fost supuși hipoxiei, administrarea de nucleozide exogene a avut un efect protector asupra miocardului ischemic. Nucleozidele au îmbunătățit probabil metabolismul azotului prin stimularea sintezei de fosfat cu energie ridicată. 15
Pe de altă parte, la șobolanii supuși hepatectomiei 70%, suplimentarea cu nucleotide a crescut biosinteza proteinelor, a scăzut oxidarea aminoacizilor și a îmbunătățit echilibrul azotului atât în ficat, cât și în mușchi. Cu toate acestea, catabolismul proteinelor nu a fost încetinit. 9
Formularea soluțiilor nutritive îmbogățite în nucleotide
S-au dezvoltat soluții nutritive enterale sau parenterale îmbogățite cu nucleotide din rezultatele preclinice. În timp ce un extract de ARN brut este suficient pentru nutriția enterală, experimentele preliminare pe animale au arătat că profilul amestecului și tipul de nucleotide administrate joacă un rol important în nutriția parenterală. 16 Nucleozidele purinice, cum ar fi adenozina și guanozina, sunt deosebit de instabile in vivo. Prin urmare, acestea sunt înlocuite cu nucleotide de purină fosfat. În plus, inozina este utilizată în locul AMP, deoarece aceasta din urmă provoacă hipotensiune și bradicardie in vivo. 14 În cele din urmă, cel mai potrivit amestec de nucleotide pentru o formulare parenterală a fost definit ca conținând inozină (29,83 mmol/l), guanozină-5-monofosfat (29,96 mmol/l), citidină (30,01 mmol/L), uridină (22,52 mmol/L) ) și timidină (7,43 mmol/L) la un raport molar de 4: 4: 4: 3: 1. 1.14.17
Studii clinice de evaluare a soluțiilor nutritive îmbogățite în nucleotide
Limitări ale utilizării clinice a nucleotidelor
Deși toate aceste observații demonstrează potențialul imunomodulator complet al unui astfel de amestec de nutrienți, în prezent nu este posibil să se evalueze rolul pe care îl joacă nucleotidele în efectele clinice. Într-adevăr, s-a sugerat recent că formulările fortificate pot fi asociate cu o mortalitate și o rată mai mare de complicații la pacienții cu terapie intensivă. 24 Cu toate acestea, studiile preclinice indică în mod clar că administrarea de nucleotide singure poate modula proliferarea populațiilor de celule cu rotație rapidă, cum ar fi leucocitele și enterocitele. Prin urmare, avem dreptul să ne întrebăm ce impact ar putea avea nucleotidele asupra concentrării celulelor canceroase, în special după intervenția chirurgicală la pacienții cu cancer gastrointestinal, deoarece aceste formulări îmbogățite sunt administrate în mod specific acestui tip de pacient. Pe de altă parte, studiile preclinice au arătat că anumite nucleotide, cum ar fi adenozina, pot provoca reacții metabolice dăunătoare atunci când sunt injectate intravenos. Prin urmare, utilizarea nucleotidelor în nutriția clinică trebuie luată în considerare cu prudență.
Concluzie
Nucleotidele nu sunt considerate substanțe nutritive esențiale. Cu toate acestea, pot deveni astfel, în timpul stresului metabolic sau al recrutării celulare rapide, în care sinteza de novo nu mai este suficientă pentru a acoperi nevoile celulare. Studiile preclinice au arătat că o sursă exogenă de nucleotide stimulează răspunsul imun celular și trofismul intestinal. Rezultatele clinice obținute cu un amestec de nucleotide și alți nutrienți confirmă aceste rezultate, dar arată că utilizarea lor ar putea prezenta riscuri pentru anumite tipuri de pacienți.
- Știri și provocări despre psoriazis în 2015 - Swiss Medical Review
- Medicamente psihotrope și greutate - Swiss Medical Review
- Pullularea bacteriană a intestinului subțire - Swiss Medical Review
- Prevenirea și vindecarea diabetului este posibilă Swiss Medical Journal
- Managementul hepatitei cronice B este o provocare în continuă evoluție - Swiss Medical Review